近日,海南大学生命健康学院病媒生物学团队在 《Insect Science》上发表了题为“miR-11903a modulates CLIPB9-mediated pathogen defense and longevity in Aedes aegypti”的最新研究成果,系统分析了miRNA对埃及伊蚊(Aedes aegypti)免疫相关基因CLIPB9的靶向调控作用以及对寿命的影响。

图1.文章首页标题及作者截图
埃及伊蚊是传播登革热等多种疾病的主要媒介,对全球公共卫生安全造成严重威胁。蚊子的先天免疫机制,尤其是黑化反应(melanization),是其抵抗病原体的核心防线:通过激活一系列CLIP结构域丝氨酸蛋白酶(CLIP domain serine proteases, CLIPs),将无活性的酚氧化酶原(prophenoloxidases, PPOs)转化为活性的酚氧化酶(phenoloxidases, POs),生成黑色素以包裹和杀灭病原体。黑化反应中会产生活性氧、多巴胺醌等有毒副产物,一旦失控会导致蚊体自身组织损伤并缩短其寿命,目前对其中调控机制的研究相对有限。既往研究已明确 miRNA 是一类非编码小 RNA ,可通过靶向 mRNA 的3'非翻译区(3'UTR)抑制基因的表达。在此基础上,研究团队发现名为miR-11903a的miRNA可以靶向调控埃及伊蚊 AeCLIPB9 基因表达,在免疫防御和寿命调节中发挥作用,为蚊媒疾病防控提供新靶点。
首先,研究团队通过生物信息学预测与双荧光素酶报告实验,发现从3 个候选 miRNA 中筛选出的 miR-11903a可特异性结合 AeCLIPB9 基因的 3'UTR区域。随后进行了体内调控验证,向雌蚊胸腔注射 miR-11903a 激动剂后,AeCLIPB9 基因表达显著下调;而注射抑制剂则表达上调,明确二者存在负调控关系。
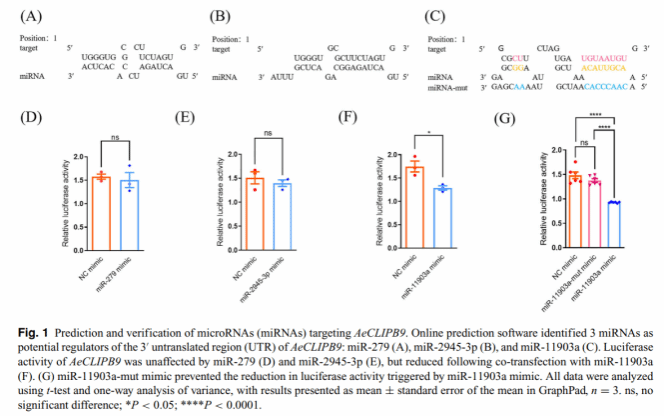
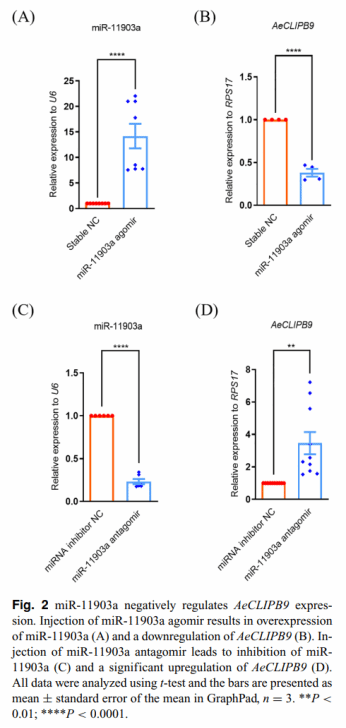
图2. miR-11903a 靶向 AeCLIPB9 的预测与验证
借助时空表达模式分析,发现 miR-11903a 在 4 龄幼虫期表达量最高,蛹期和成虫期逐步下降;在雌蚊成虫中,其在翅膀、头部和中肠富集。通过病原体侵染实验联合qPCR 分析,观察到侵染之后 AeCLIPB9 表达显著上调,而 miR-11903a 表达明显下降,二者趋势完全相反,证实该调控通路参与蚊虫先天免疫。
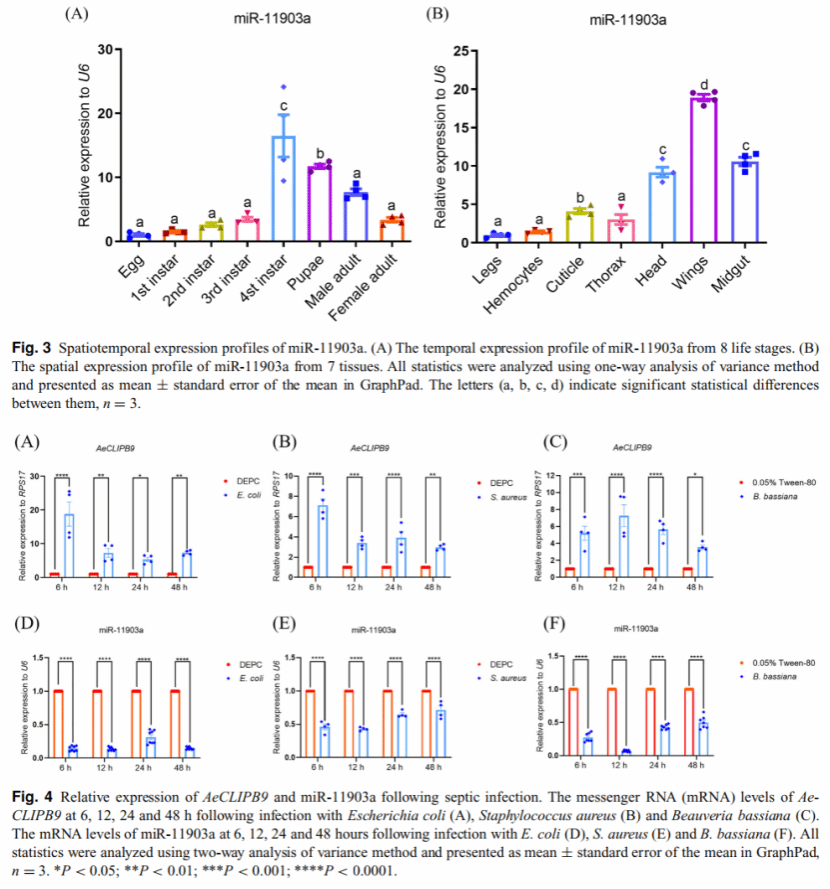
图3. miR-11903a 的时空表达模式及病原体侵染后
AeCLIPB9 与 miR-11903a 的表达变化
RNA 干扰与 7 天生存实验发现,敲低 AeCLIPB9 会显著提升蚊虫对病原体的易感性;注射 miR-11903a 激动剂可产生类似效果,而注射抑制剂虽激活 AeCLIPB9,但蚊虫存活率降低,可能是由于过度黑化反应反而导致蚊体损伤。在寿命调节研究中,团队通过RNA 干扰、共注射实验和寿命监测发现,丝氨酸蛋白酶抑制剂AeSerpin-2 缺失会因过度黑化缩短蚊虫寿命,而敲低 AeCLIPB9 或注射 miR-11903a 激动剂可部分挽回寿命损失;反之,注射 miR-11903a 抑制剂会进一步缩短 AeSerpin-2 缺失蚊虫的寿命,证实 miR-11903a 通过调控 AeCLIPB9 介导的黑化反应,维持蚊虫免疫与寿命的平衡。
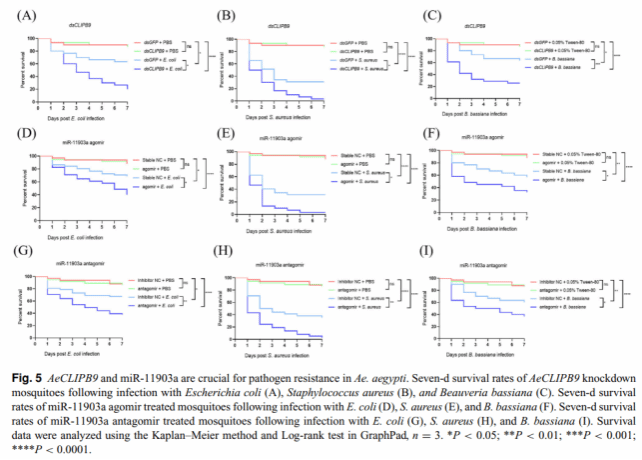
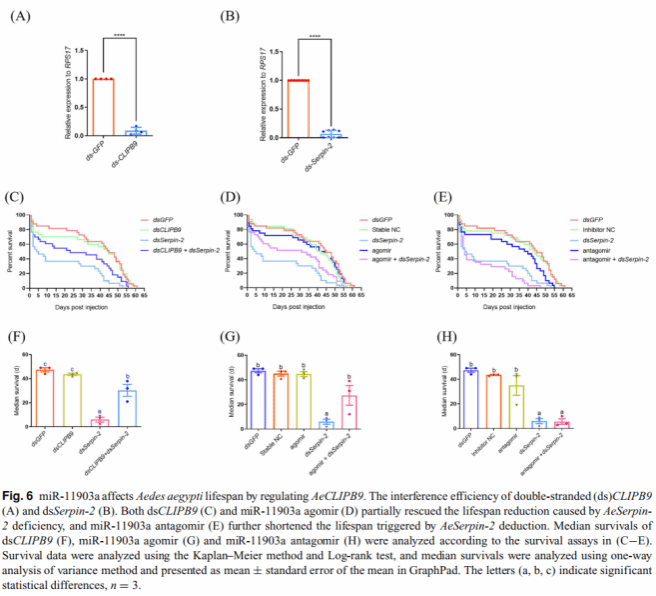
图4. AeCLIPB9 与 miR-11903a 在蚊虫抗病原体中的作用验证
及蚊虫寿命影响研究
海南大学生命健康学院博士研究生刘焱晖为该论文的第一作者。海南大学生命健康学院病媒生物学团队韩谦教授为该论文的通讯作者。此项工作得到了国家自然科学基金(U22A20363)、海南省重大科技计划(ZDKJ2021035)以及海南省研究生创新科研项目(Qhyb2022-41)的支持。
论文链接:https://doi.org/10.1111/1744-7917.13512
