2025年1月17日,海南大学生命健康学院免疫调控与成像团队在ACS Nano上发表了题为“Targeted Modulation of the Meningeal Lymphatic Reverse Pathway for Immunotherapy of Breast Cancer Brain Metastases”的最新研究成果,通过前颈部皮下注射靶向调节脑膜淋巴系统的纳米探针,实现了脑膜淋巴系统的三维成像以及乳腺癌脑转移免疫治疗。

论文链接:https://pubs.acs.org/doi/10.1021/acsnano.4c15860
脑膜淋巴管参与中枢神经系统免疫监视和免疫反应,在多种神经疾病的发生与发展中扮演着重要角色。尽管目前对脑膜淋巴管的基本结构和功能解析逐步有所认识,然而对脑膜淋巴管的完整三维空间分布结构、淋巴循环信息及其免疫调节功能尚不完全清楚,并缺乏靶向调节脑膜淋巴系统免疫功能的方法。因此,发展脑膜淋巴系统靶向标记与调控的方法,实现脑膜淋巴系统的三维空间分布成像和脑疾病的免疫调控,将有助于我们理解中枢神经系统的免疫功能并提出治疗新策略。
在这项针对脑膜淋巴系统的最新研究工作中,研究人员研制了一种具有清道夫受体B1靶向能力的CT/荧光多功能纳米探针α-PLNP,通过不同位点的注射,实现了脑膜淋巴系统通路的正向和逆向长程示踪。小鼠小脑延髓池注射α-PLNP后,CT成像较完整地展示小鼠脑膜淋巴管-颈部淋巴结的三维空间分布结构信息;而采用小鼠前颈部皮下注射α-PLNP后,α-PLNP能够绕过血脑屏障限制经颈部淋巴结-脑膜淋巴管轴到达大脑。进而,在α-PLNP的基础上,研究人员进一步发展了携带具有免疫调节功能的蜂毒肽纳米药物α-M-PLNP,小鼠前颈部皮下注射α-M-PLNP能够有效抑制乳腺癌脑转移,并显著延长小鼠存活时间。流式分析结果显示,α-M-PLNP治疗后,既能显著提升脑组织中Ki67+CD8+ T细胞的数量,又能降低CD4+Foxp3+ Treg细胞的比例。而对于颈部淋巴结,α-M-PLNP治疗能够促进淋巴结中IFN-γ+CD8+ T细胞和IFN-γ+CD4+ T细胞的比例显著升高,同时也提高了TNF-α+CD8+ T细胞和TNF-α+CD4+ T细胞的比例。更重要的是,α-M-PLNP还能活化颈部淋巴结中的抗原递呈细胞重塑淋巴结微环境,进而诱导显著的抗肿瘤免疫反应。
综上所述,该研究提出了一种新颖的脑肿瘤免疫治疗新方法,通过对脑膜淋巴系统逆行通路进行靶向免疫调节,绕过血脑屏障的限制性,实现了乳腺癌脑转移的免疫调控。该研究为深入了解中枢神经系统脑膜淋巴系统的结构和功能提供新方法,为中枢神经系统相关疾病的诊断与治疗提供新策略。
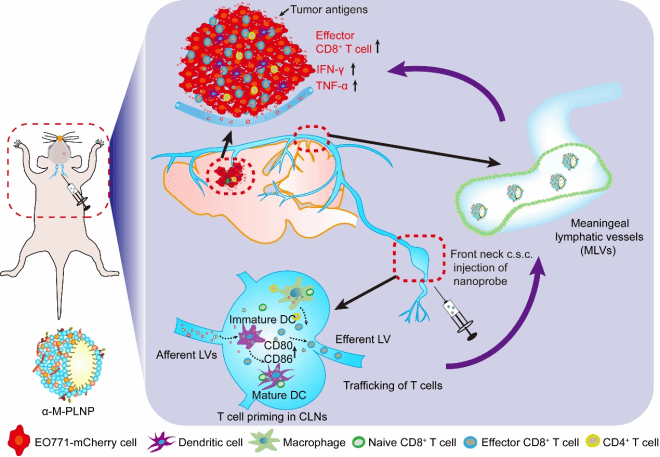
图1. 通过逆向途径靶向调节脑膜淋巴系统实现乳腺癌脑转移免疫治疗
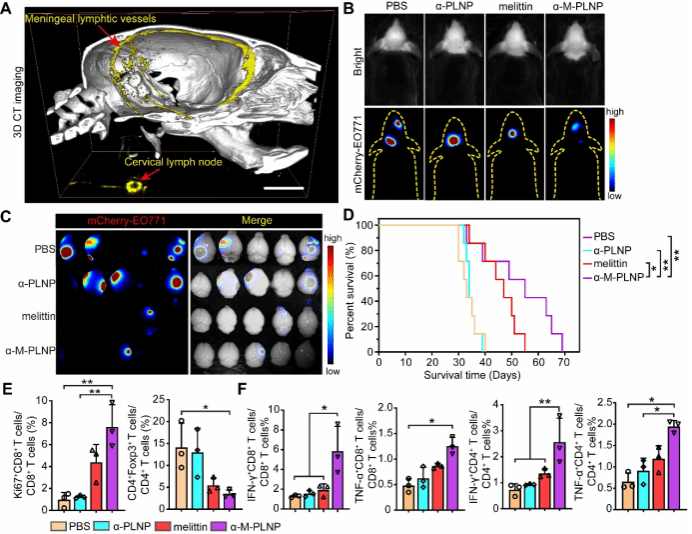
图2. 脑膜淋巴系统成像及乳腺癌脑转移免疫调控作用。(A)脑膜淋巴系统三维CT成像;(B)活体荧光成像监测前颈部皮下注射α-M-PLNP的乳腺癌脑转移抑制作用;(C)乳腺癌脑转移的离体荧光成像;(D)不同治疗组小鼠生存率曲线;(E)流式定量分析不同治疗组脑内Ki67+CD8+ T细胞和CD4+Foxp3+ Treg细胞的比例;(F)流式定量分析颈部淋巴结内CD8+和CD4+ T细胞中IFN-γ和TNF-α表达水平。
海南大学生命健康学院和生物医学工程学院戴艳锋副研究员和余祥教授为该论文的共同第一作者。海南大学生命健康学院的张智红教授和生物医学工程学院刘谦教授为该论文的共同通讯作者。该项研究的参与者还包括华中科技大学和海南大学的研究人员,并得到国家自然科学基金项目(32227801, 32201131)、海南省科技人才创新项目(KJRC2023B09)、海南大学科研基金(KYQD(ZR)20078)和WNLO创新基金的资助。
